Oxyacid, всяка киселина, съдържаща кислород. Повечето ковалентни неметални оксиди реагират с вода и образуват киселинни оксиди; което означава, че реагират с вода за образуване оксикиселини че добив хидрониев йони (H 3 О +) в разтвор. Има някои изключения, като въглероден окис, CO, азотен оксид, N 2 О и азотен оксид NO.
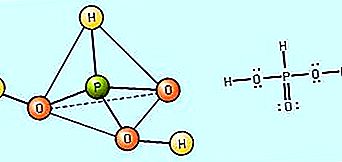
Силата на оксакиселината се определя от степента, в която се дисоциира във вода (т.е. способността й да образува Н + йони). Като цяло относителната сила на оксиацидите може да се прогнозира въз основа на електроотрицателността и окислителния номер на централния неметален атом. Силата на киселината се увеличава с увеличаването на електроотрицателността на централния атом. Например, тъй като електроотрицателност на хлор (Cl) е по-голяма от тази на сяра (S), който на свой ред е по-голяма от тази на фосфор (Р), може да се прогнозира, че перхлорна киселина, HClO 4, е по-силна киселина от сярна киселина, H 2 SO 4, който трябва да бъде по-силна киселина от фосфорна киселина, H 3 PO 4, За даден неметален централен атом силата на киселината се увеличава с увеличаването на окислителното число на централния атом. Например, азотна киселина, HNO 3, в които азотът (N) атом има окисление на 5, е по-силна киселина от азотиста киселина, HNO 2, където състоянието на азот окисляване е три. По същия начин, сярна киселина, H 2 SO 4, със сяра в 6 окисление, е по-силна киселина от сярна киселина, H 2 SO 3, където съществува 4 окисление на сяра.
Солта на оксакиселината е съединение, образувано, когато киселината реагира с основа: киселина + основа → сол + вода. Този тип реакция се нарича неутрализация, тъй като разтворът се прави неутрален.