Родий (Rh), химичен елемент, един от платинените метали от групи 8-10 (VIIIb), периоди 5 и 6 от периодичната таблица, използван предимно като легиращ агент за втвърдяване на платина. Родий е скъпоценен, сребристо-бял метал, с висока отражателна способност за светлина. Не се корозира или опетнява от атмосферата при стайна температура и често се поставя върху метални предмети и се полира, за да даде постоянни, привлекателни повърхности за бижута и други декоративни изделия. Металът също се използва за производство на отразяващи повърхности за оптични инструменти.
Родият, добавен към платината в малки количества, дава сплави, които са по-твърди и губят тегло при високи температури дори по-бавно от чистата платина. Такива сплави се използват за лабораторни тигели за пещи, електроди за свещи и катализатори в много гореща химическа среда (включително автомобилни каталитични конвертори). При промишленото производство на азотна киселина се използват марлеви катализатори от родиево-платинени сплави, тъй като те могат да издържат на температурата на пламъка, тъй като амонякът се изгаря до азотен оксид. Тел от сплав, 10 процента родий - 90 процента платина, присъединен към жица от чиста платина, образува отлична термодвойка за измерване на високи температури в окисляваща атмосфера. Международната температурна скала се определя в областта от 660 ° до 1,063 ° С (1,220 ° до 1,945 ° F) от електромоторната сила на тази термодвойка.
Родий е рядък елемент, съдържащ до 4,6 процента от естествените платинени сплави. Среща се и в естествени сплави на иридий и осмия: до най-малко 11,25 процента в иридосмин и до най-малко 4,5 процента в сизерскит. Родийът се среща в природата във връзка с останалите платинени метали и отделянето и усъвършенстването му са част от цялостната металургична обработка на групата. Родият обикновено се получава в търговската мрежа като страничен продукт от извличането на никел и мед от техните руди.
Естественият родий се състои изцяло от стабилен изотоп родий-103. Елементът за първи път е изолиран (1803 г.) от сурова платина от английския химик и физик Уилям Хайд Уолъстън, който го кръсти от гръцкия родон („роза“) за червения цвят на редица съединения. Родий е силно устойчив на атака от киселини; масивният метал не се разтваря от горещо концентрирана азотна или солна киселина или дори от акварегия. Металът се разтваря в кондензиран калиев хидрогенсулфат, за да се получи сложен водоразтворим сулфат K 3 Rh (SO 4) 3 · 12H 2 O, в гореща концентрирана сярна киселина и в концентрирана солна киселина, съдържаща натриев перхлорат при 125 ° -150 ° С (257 ° -302 ° F).
Родиевата химия се фокусира главно върху окислителните състояния +1 и +3; няколко съединения от другите положителни окислителни състояния чрез +6 се разпознават. Родий образува диродиев тетраацетат, Rh 2 (O 2 CCH 3) 4 и различни производни, съдържащи две допълнителни лиганди, например, вода, пиридин, или трифенилфосфин в окисление 2. Комплексите в състояние на окисляване +1 съдържат главно въглероден оксид, олефини и фосфини като лиганди. Всички родиеви съединения лесно се редуцират или разлагат чрез нагряване, за да се получи прахообразният или гъбен метал. Сред тези съединения, родиев трихлорид, RhCl 3 (в която родий е в състояние 3), е един от най-важните. Той осигурява изходен материал за много от други родиеви съединения в различни окислителни състояния. Във водни емулсии той може да катализира редица полезни органични реакции.
Свойства на елемента
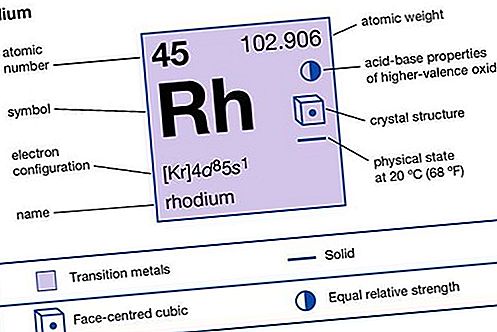
| атомно число | 45 |
|---|---|
| атомно тегло | 102.905 |
| точка на топене | 1,966 ° C (3,571 ° F) |
| точка на кипене | 3,727 ° C (6,741 ° F) |
| специфична гравитация | 12.4 (20 ° C) |
| окислителни състояния | +1, +2, +3, +4, +5, +6 |
| конфигурация на електрон. | [Kr] 4d 8 5s 1 |













