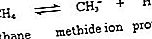Сярен диоксид, (SO 2), неорганично съединение, тежък, безцветен, отровен газ. Произвежда се в огромни количества в междинни етапи на производство на сярна киселина.

замърсяване на въздуха: серен диоксид
Безцветен газ с остър, задушаващ мирис, серен диоксид се образува при изгарянето на въглища или масло, които съдържат сяра като примес.
Серен диоксид има остър, дразнещ мирис, познат като миризма на току-що ударен мач. Възникващ в природата във вулканични газове и в разтвор във водите на някои топли извори, серен диоксид обикновено се получава промишлено чрез изгарянето във въздух или кислород на сяра или такива съединения на сяра като железен пирит или меден пирит. При изгарянето на серосъдържащи горива се образуват големи количества серен диоксид. В атмосферата може да се комбинира с водна пара и да образува сярна киселина, основен компонент на киселинния дъжд; през втората половина на XX век широко се приемат мерки за контрол на киселинните дъждове. Серен диоксид е предшественик на триоксид (SO 3) използва за сярна киселина. В лабораторията газът може да бъде получен чрез намаляване на сярна киселина (H 2 SO 4) до сярна киселина (H 2 SO 3), която се разлага във вода и серен диоксид, или чрез третиране на сулфити (соли на сярна киселина) със силни киселини, като солна киселина, като отново образува сярна киселина.
Сярният диоксид може да се втечнява при умерено налягане при стайна температура; течността замръзва при -73 ° C (−99.4 ° F) и кипи при -10 ° C (14 ° F) при атмосферно налягане. Въпреки че основните му приложения са в приготвянето на сярна киселина, серен триоксид и сулфити, серен диоксид също се използва като дезинфектант, хладилен агент, редуциращ агент, белина и хранителен консервант, особено в сушените плодове.