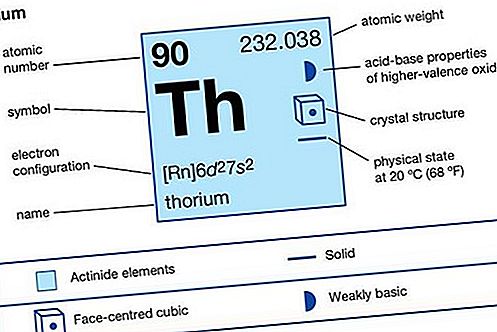
Торий (Th), радиоактивен химичен елемент от актиноидната серия на периодичната таблица, атомен номер 90; това е полезно ядрено реакторно гориво. Ториумът е открит (1828 г.) от шведския химик Йонс Яков Берзелий. Той е сребристо бял, но става сив или черен при излагане на въздух. Той е около половината по-обилен от оловото и е три пъти по-обилен от урана в земната кора. Торият се възстановява търговски от минерала моназит и се среща и в други минерали като торит и торианит. Торий метал е произведен в търговски количества от редукция на тетрафлуорид (THF 4) и двуокис (ThO 2) и чрез електролиза на тетрахлорид (ThCl 4). Елементът е кръстен на норвежкия бог Тор.

актиноиден елемент: Практически приложения на актиноидите
Ториумът също има потенциално голяма икономическа стойност, тъй като един от неговите изотопи, торий-232, може да бъде превърнат в
Металът може да бъде екструдиран, валцуван, кован, преместван и завъртян, но изтеглянето е трудно поради ниската якост на опън на тория. Това и други физични свойства като точки на топене и кипене са силно повлияни от малки количества от някои примеси, като въглерод и ториев диоксид. Торий се добавя към магнезий и магнезиеви сплави за подобряване на тяхната високотемпературна якост. Използва се в търговски фотоелектрически клетки за измерване на ултравиолетова светлина с дължина на вълната, варираща от 2000 до 3750 ангстрема. Добавен към стъклото, торият дава очила с висок коефициент на пречупване, полезни за специализирани оптични приложения. Преди това е бил с голямо търсене като компонент на мантии за газови и керосинови лампи и е използван при производството на волфрамови нишки за електрически крушки и вакуумни тръби.
Радиоактивността на торий е открита независимо (1898) от немския химик Герхард Карл Шмит и от френския физик Мари Кюри. Естественият торий е смес от радиоактивни изотопи, предимно много дълговечния торий-232 (1,40 × 10 10 -годишен полуразпад), родител на серията радиоактивни гниения на тория. Други изотопи се срещат естествено в серията на гниене на уран и актиний, а торият присъства във всички уранови руди. Торий-232 е полезен в развъдните реактори, тъй като при улавяне на бавно движещи се неутрони той се разпада в делящ се уран-233. Приготвени са синтетични изотопи; торий-229 (период на полуразпад 7,880 г.), образуван във веригата на разпад, произхождащ от синтетичния актиноиден елемент нептуний, служи като следа за обикновения торий (торий-232).
Торият проявява окислително състояние от +4 в почти всички свои съединения. Th 4+ йонът образува много сложни йони. Диоксидът (ThO 2), много огнеупорно вещество, има много индустриални приложения; ториев нитрат се предлага като търговска сол.
Свойства на елемента
| атомно число | 90 |
|---|---|
| атомно тегло | 232.038 |
| точка на топене | около 1700 ° C (3100 ° F) |
| точка на кипене | около 4000 ° C (7,200 ° F) |
| специфична гравитация | около 11,66 (17 ° C) |
| окислително състояние | 4 |
| електронна конфигурация на газообразно атомно състояние | [Rn] 6d 2 7s 2 |