Иридий (Ir), химичен елемент, един от платинените метали от групи 8-10 (VIIIb), периоди 5 и 6 от периодичната таблица. Той е много плътен и рядък и се използва в платинени сплави. Ценен, сребристо-бял метал, иридий е твърд и чуплив, но става пластичен и може да се работи при бяла топлина, от 1200 ° до 1500 ° C (2,200 ° до 2700 ° F). Той е едно от най-гъстите сухоземни вещества. В масово състояние металът е практически неразтворим в киселини и не се атакува дори от акварегия. Може да се разтвори в концентрирана солна киселина в присъствието на натриев перхлорат при 125 ° С до 150 ° С (257 ° до 302 ° F).
Поради трудностите при подготовката и производството, чистият метал има малко приложения. Иридий се използва главно под формата на платинени сплави. Платиново-иридиевите сплави (5 до 10 процента иридий) са лесно обработваеми метали, които са много по-твърди и по-твърди и по-устойчиви на химическа атака от меката чиста платина. Такива сплави се използват за бижута, химикалки, хирургически щифтове и шарнири, както и за електрически контакти и искри. Международният прототип на стандартен килограм маса е направен от сплав, съдържаща 90 процента платина и 10 процента иридий.
Чистият иридий вероятно не се среща в природата; неговото изобилие в земната кора е много малко, около 0,001 части на милион. Макар и рядко, иридийът се среща в естествени сплави с други благородни метали: в иридосмин до 77 процента иридий, в платиноридий до 77 процента, в ауросмиридий 52 процента, и в естествена платина до 7,5 процента. Обикновено иридийът се произвежда търговски заедно с другите платинени метали като страничен продукт при производството на никел или мед.
Руди, съдържащи иридий, се намират в Южна Африка и Аляска, САЩ, както и в Мианмар (Бирма), Бразилия, Русия и Австралия. В края на 20 век Южна Африка е основният световен производител на иридий.
Елементът е открит през 1803 г. в неразтворимите в киселина остатъци от платинени руди от английския химик Смитсън Тенант; френските химици Х.-В. Collet-Descotils, A.-F. Fourcroy и N.-L. Вокелин го идентифицира приблизително по едно и също време. Името иридий, получено от гръцката дума iris („дъга“), се отнася до различните цветове на неговите съединения. Естественият иридий се състои от смес от два стабилни изотопа, иридий-191 (37,3%) и иридий-193 (62,7%). Химията на иридиума се концентрира върху окислителни състояния от +1, +3 и +4, въпреки че съединенията от всички състояния от 0 до +6 са известни с може би изключение от +2. Комплексите в състояние на окисляване +1 съдържат главно въглероден оксид, олефини и фосфини като лиганди. Анионите хексахлороиридат, [IrCl 6] 2− и хексабромооридатът [IrBr 6] 2− са единствените забележими химически видове, съдържащи иридий в състояние на окисление +4. Иридий е малко по-реактивен от рутения и осмия.
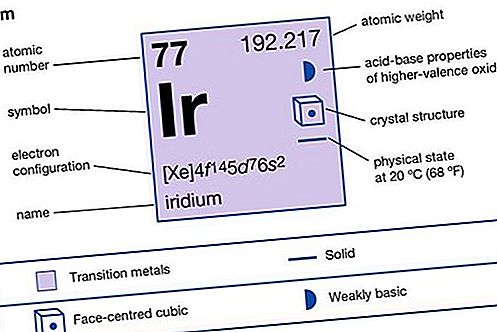
Свойства на елемента
| атомно число | 77 |
|---|---|
| атомно тегло | 192,2 |
| точка на топене | 2,410 ° C (4,370 ° F) |
| точка на кипене | 4,527 ° C (8,181 ° F) |
| специфична гравитация | 22.4 (20 ° C) |
| окислителни състояния | +1, +3, +4 |
| конфигурация на електрон. | [Xe] 4f 14 5d 9 |